70以上 元素周期表 价数 460744-元素周期表 价数
下列关于元素在周期表中位置的叙述正确的是 A.原子的最外层有2个电子的元素一定是ⅡA族元素 B.元素所在的主族序数与最外层电子数之比为1的元素都是金属元素 C.俄罗斯专家首次合成了 X原子,116号元素位于元素周期表中第七周期ⅥA族 D.原子最外层元素周期表与元素周期律试题分享梳理文档资料 PAGE页码 11 NUMPAGES总页数 11 文档资料整理不易仅供学习参考谢谢元素周期表与元素周期律一选择题1.金属钛对人体体液无毒且有惰性能与肌肉和骨骼生长在一起有生物金属之称.下列有关 eqoal42 Ti和 eqoal5022 Ti的说法中正确的是 A eqoal42 Ti和 eqoal5022 Ti的质量数相同互称为同位素B eqoal42 Ti和 eqoal5022 Ti的质子数相同互称同104 rader d区元素是指周期表中第3~12,即III B、IV B、V B、VI B、VIII、I B和II B族的元素,共有30种金属元素,其价电子构型为(n1)d 1~10 ns 1~2 ,因为位于典型的金属元素(s区元素)与典型的非金属元素(p区元素)之间,d区元素和f区元素又共称为过渡元素或过渡金属。
化学从宏观和微观两个角度认识物质 1 图甲是两种元素在元素周期表 中的信息 图乙是钠原子和氧原子的原子结构示意图 图甲的横线上填的是nana 图乙横线上的数字是66 根据图乙的信息 写出氧化钠的化学式并标出化合价 1na2 2o 1na2 2o 2 下 表所列的是部分元素的有关
元素周期表 价数
元素周期表 价数- 元素周期表有7个周期,16个族。 每一个横行叫作一个周期,每一个纵行叫作一个族(VIII B族包含三个纵列)。 这7个周期又可分成短周期(1、2、3)、长周期(4、5、6、7)。 共有16个族,从左到右每个纵列算一族(VIII B族除外)。 例如:氢属于I A族元素,而氦属于0族元素。 同一周期内,从左到右,元素核外电子层数相同,最外层电子数依次递增,原子半径一、元素周期表的分区及化合价规律 1元素周期表与元素周期律的关系 元素周期律的发现,对化学的发展有很大影响。_____是_____的表现形式,反映了元素之间的_____,是学习、研究、应用化学的一种重要工具。 2元素周期表的金属区和非金属区




科学家推出更新的元素周期表 门捷列夫 大纪元
周期数等于电子层数 原子结构、元素性质及元素在周期表中位置三者的关系 1.原子结构与元素在周期表中的位置关系 ⑴核外电子层数 == 周期数 ⑵主族元素的最外层电子数 == 价电子数 == 主族序数 == 最高正价数 ⑶质子数 == 原子序数 == 原子核外电子数 == 核电荷数 ⑷负价绝对值 == 8 – 主族数(限 12元素化合价 周期外,同周期从左到右,元素最高正价由碱金属1 递增到7,非金属元素负价由碳族4 递增到1(氟无 13单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减; (2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增 14元素的金属性与非金属性 15最高价氧化物和水 元素周期表习题_高二理化生_理化生_高中教育_教育专区 9.已知 1~18 号元素的离子 aW3+、bX+、cY2-、dZ-都具有相同电子层结构,下列关系 正确的是 ( ) A.质子数:c>d B.离子的还原性:Y2->Z- C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W 11. A、B 两元素为某周期ⅡA 族和ⅢA 族元素,若 A 元 9.已知 1~18 号元素的离子 aW3+、bX+、cY2-、dZ-都具有相同
化学元素周期表与化合价我们的老师说元素周期表中:一般主族序数为奇数的族内元素化合价主要是奇数,主族序数为偶数的族内元素化 1年前 5个回答 为什么锑、铋 沸点反常氮族元素在化学元素周期表中,自上而下,元素的沸点一个比一个高,但是锑、铋却一下子低下来,请问这是为下表是部分短周期元素的原子半径及主要化合价,根据表中的信息,判断下面叙述正确的是 元素代号 l m q r t 原子半径(nm) 0160 0143 00 0102 0074 主要化合价 2 3 2 6、2 2 a.l2与r2的核外电子数相等 b.m与t形成的化合物具有两性c.单质与同浓度的稀盐酸反应的速率为q>l d.r与t的氢 元素周期表中共有 118 种元素。每一种元素都有一个编号,大小恰好等于该元素原子的核内电子数目,这个编号称为原子序数。 原子的核外电子排布和性质有明显的规律性,科学家们是按原子序数递增排列,将电子层数相同的元素放在同一行,将最外层电子数
元素周期表 是依 原子序数 、 核外电子排布 情况和 化学性质 的相似性来排列 化学元素 的表格。 元素周期表、化学式与化合价专项复习学案 1 部分包含数学公式或PPT动画的文件,查看预览时可能会显示错乱或异常,文件下载后无此问题,请放心下载。 2 本文档有教师用户上传,莲山课件网负责整理代发布。 如果您对本文档有争议请及时联系客服。 3 想要完全集齐所有的元素,究竟需要多少钱呢? 事实上要收集齐这些元素,需要的金钱是难以想象的,就连世界前首富比尔盖茨都都买不起所有的元素,而且在元素周期表上还有不少元素都是属于有价无市的存在,并不是有钱就能买得到的。 同时还有一些放射性元素,就算不去考虑它对人体的伤害,那也由于它的不稳定性,我们也无法对其进行储存。 就拿比尔




高一化学必修第一册19版 第四章第一节原子结构与元素周期表 三好网



1
元素周期表简图 区的名称来自按照构造原理最后填充的能级的符号。 元素周期表的五个分区 1、s区:含ⅠA与ⅡA共两族两列;价电子层为ns1或2 (n≥1)。 特点:价电子数=主族序数=最外层电子数 注意①并不是所有价电子层为ns1或2的元素都在S区, He除外(它在p区) ②除H外,都是金属元素 2、p区:含ⅢA至ⅦA及零族共六族六列;价电子层为ns2 np16 (n≥2) 。 特点B 元素正二价离子结构和 Ne 具有相同的电子层结构。 58g B 的氢氧化物恰好能与 100mL 2mol/L 的盐酸完全中和。 H 2 在 C 单质中燃烧产生苍白色火焰。 D 原子的最外层电子数是次外层电子数的 3 倍。 ⑴ 元素 C 位于周期表第 _____ 周期 _____ 族,它的最高价氧化物的化学 元素周期表的创始人: 德米特里·伊万诺维奇·门捷列夫()是俄罗斯伟大的化学家,自然科学基本定律化学元素周期表的创始人。 概念: 根据元素的原子结构和性质,将已知的100多种元素按原子序数(数值上等于核电荷数)科学有序地排列起来所得的表,叫元素周期表。



Translated Copy Of Electron Configurations And The Table



元素周期表150岁了化学元素周期表完备化学顺口溜价位表口诀 化学元素周期表 化学 万华化学 中国化学 凯利环境集团
周期表前四周期的元素 a 、 b 、 c 、 d 、 e ,原子序数依次增大。 a 的核外电子总数与其周期数相同, b 的价电子层中未成对氮在周期表中的信息和原子结构示意图如下。 根据信息,氮元素的相对原子质量为 ,原子最外层电子数为 ;氮元素与氢元素形成的化合物中氮的化合价为 ,该物质的水溶液pH 7(填">"、"价电子数10,因此为VIIIB族元素(第10族)(元素周期表的8,9,10列均为VIIIB)。主量子数为5,因此为第五周期元素。 Eu铕, Xe 6s²4f⁷,最外的亚层是4f⁷,处在上图橙色的f分区,为镧系金属。价电子数27=9,因此为从镧开始数第7个,镧系和锕系一般不以族数
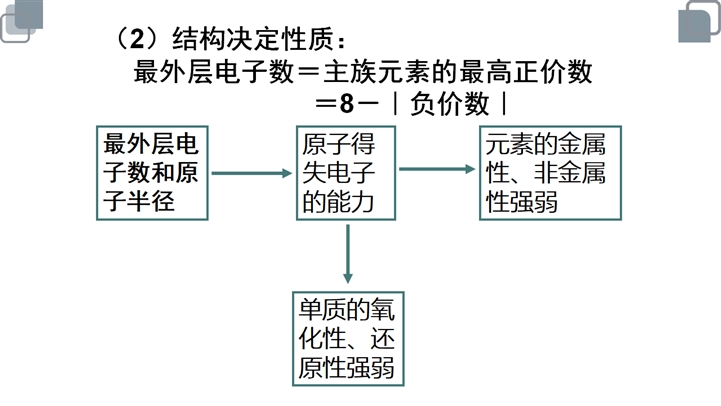



元素周期表和元素周期律的应用 Ppt课件



化学元素周期表搞笑口诀
12 元素化合价 (1)除第1周期外,同周期从左到右,元素最高正价由碱金属1递增到7,非金属元素负价由碳族4递增到1(氟无正价,氧无6价,除外); (2)同一主族的元素的最高正价、负价均相同 3/7 13 单质的熔点 (1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减; (2)同一族元素从上到下,元素组成的金属单质的熔点2 .熟练掌握周期表中的一些规律 ( 1 )各周期元素种类数 一~六周期元素种类分别为 2 、 8 、 8 、 18 、 18 、 32 ,第七周期填满也是 32 种。 ( 2 )稀有气体元素原子序数 一~六周期分别为 2 、 10 、 18 、 36 、 54 、 86 。 ( 3 )同族上、下相邻元素的原子序数相差 2 、 8 、 18 、 32 。 元素的物理、化学性质随原子序数逐渐变化的规律叫做元素周期律。 元素周期律由门捷列夫(Dmitri Mendeleyev)首先发现,并根据此规律创制了元素周期表。 结合元素周期表,元素周期律可以表述为: 随着原子序数的增加,元素的性质呈周期性的递变规律:;




元素周期表离子半径图 第1页 图说健康




化學式4 週期表上元素的根價 Youtube
周期表中16号元素和4号元素的原子相比较,前者的下列数据是后者的4倍的是 a.电子数 b.最外层电子数 c.电子层数d.次外层电子数 试题详情 1 题目(题型不定项选择题,难度简单)周期表中关于主族元素性质的叙述中不正确的是( ) A.主族序数等于原子最外层电子数 B.主族元素最高正价等于最外层电子数 C.第n主族元素其最高正价为n价,负价绝对值为8n(n≥4) D.第n主族元素其最高价氧化物对应的化学式为R2O2.元素性质的周期性变化 (1)元素主要化合价的周期性变化 规律:随着原子序数的递增,元素的最高正化合价呈现+1→+7,最低负化合价呈现-4→-1 的周期 性变化。 注意:元素化合价的"三个二" ①二"特殊" F 无正价,O 无最高正价。



元素周期表元素及化合物的递变规律



悟空问答 元素周期表中最疯狂元素是什么 23个回答
元素周期表中短周期元素原子半径最大的是Na短周期中最大的离子半径是P3原子和离子半径大小规律①核电荷数相同的微粒,电子数越多,则半径越大阳离子半径Fe2 > Fe3;Na Li > Be2 ② 与Ne电子层结构相同的微粒O2–>F–>Na>Mg2>Al3 ③ 与Ar电子层结构相同的微粒S2– > Cl– > K >Ca2 ③电子数和核电荷数元素周期律和元素周期表的综合应用专项练习,通过试题学习更好的掌握考点重点,全面把握考点做题技巧 。 a、b、d、e、f为短周期元素,非金属元素a最外层电子数与其周期数相同,b的最外层电子数是其所在周期数的2倍。 图7是部分周期元素化合价



元素周期表分区 选修3 91学



化学元素周期表打印版下载 元素周期表pdf打印版下载最新超清版 当易网




Kdcnx3ljaqevem
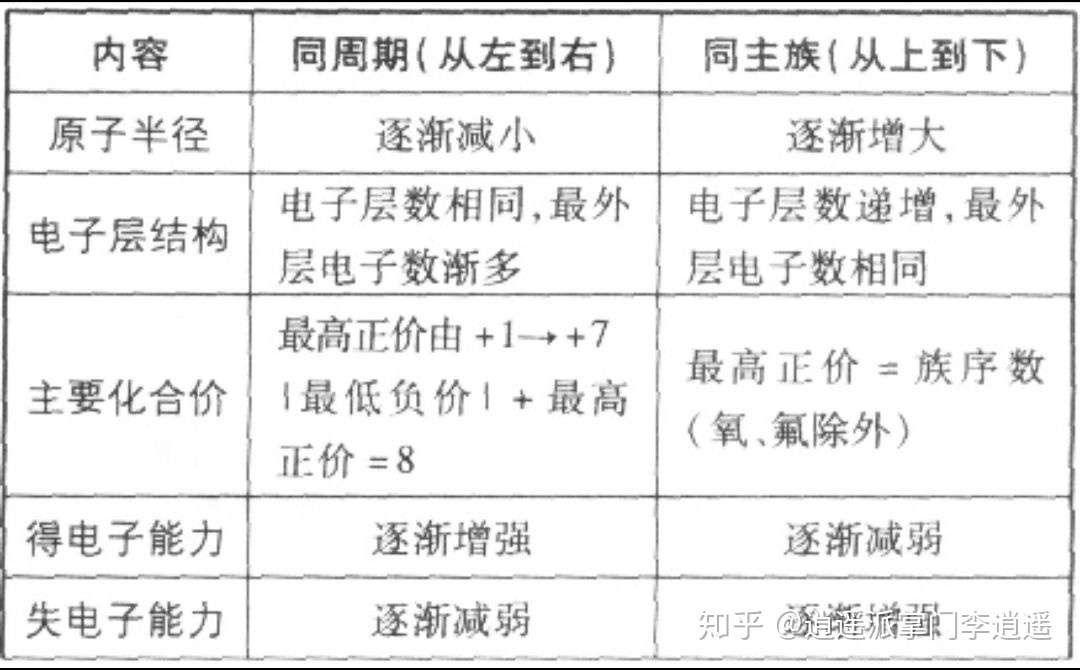



高中化学归纳必修二元素周期表及元素周期律 知乎




元素周期表软件下载 化学元素周期表软件v2 01 最新版 七喜软件园




历年物质结构元素周期律和元素周期表高考试题下载 Word模板 爱问共享资料



元素周期表 快懂百科
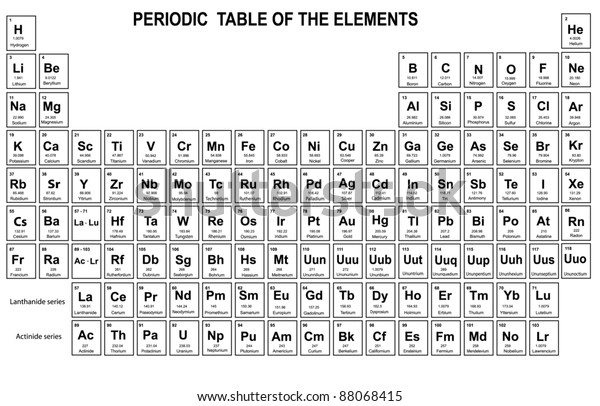



元素周期表与原子数 符号和重量库存矢量图 免版税
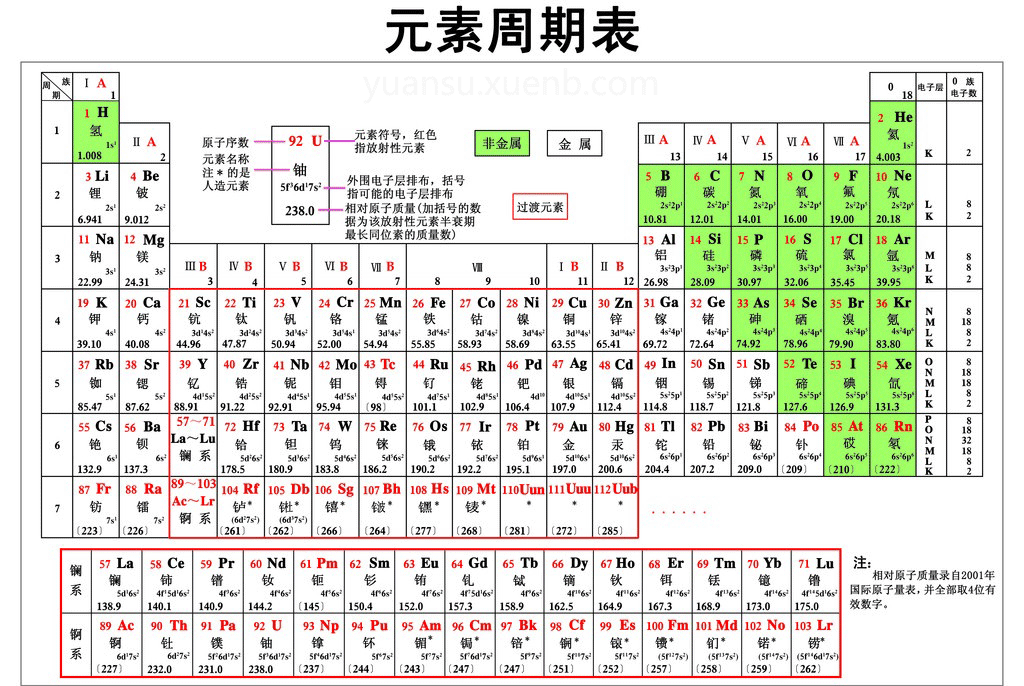



元素周期表 化学元素周期表高清图



元素周期表元素周期表口诀顺口溜 天气网



悟空问答 如果把元素周期表里所有元素都买1克 大概需要多少钱 叮当新科技的回答 0赞




元素周期表有哪些口诀 百度经验



1




元素周期表摆件价格 元素周期表摆件图片 星期三



元素周期表51号骂人元素周期表第51号元素 欧星推网




原子结构与元素周期表 物质结构元素周期律ppt 第2课时原子结构与元素的性质 Ppt课件下载 人人ppt
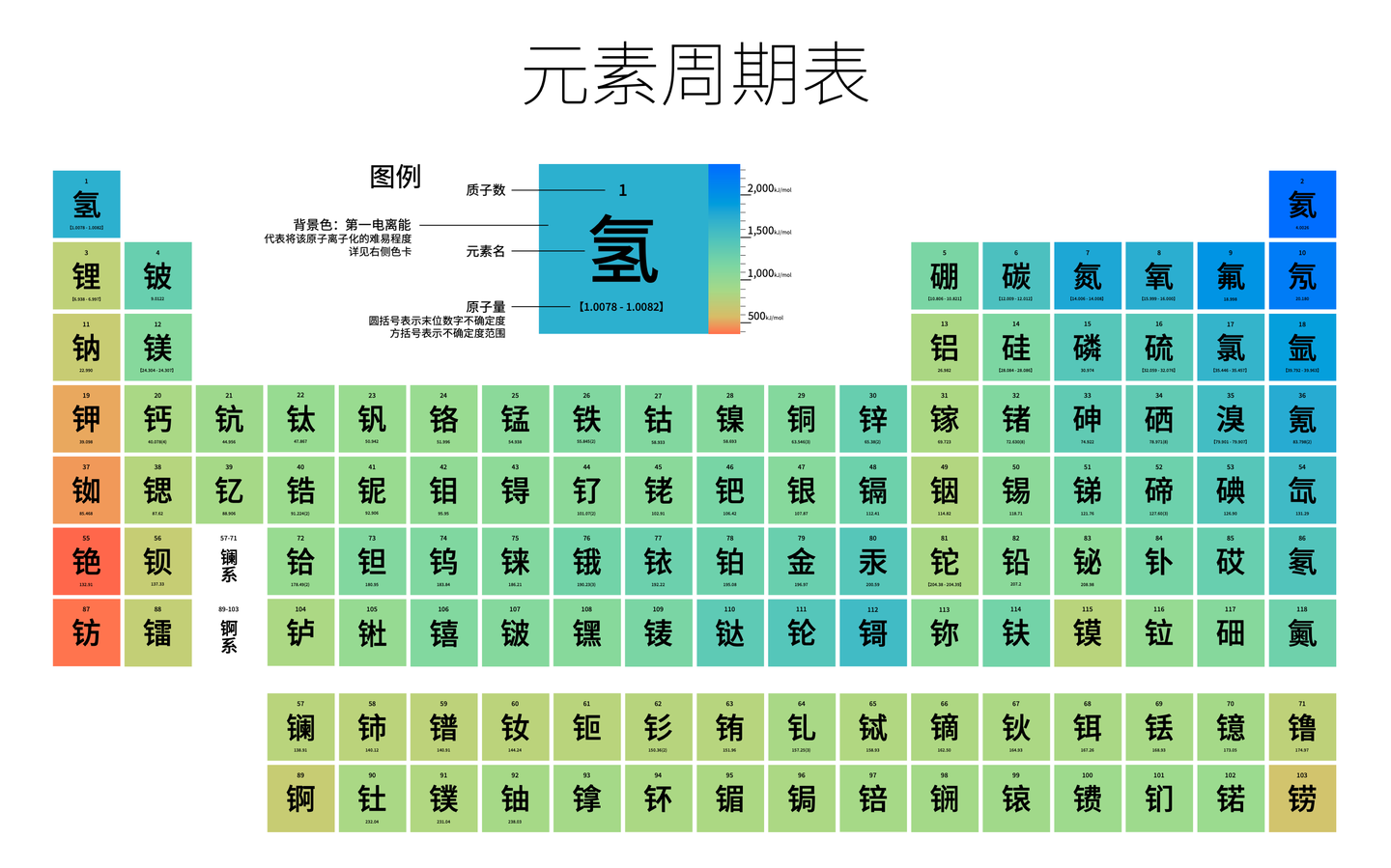



化學元素周期表第七週期齊了 談談這張表 知乎



原子结构元素周期律



元素周期律和元素周期表 原子结构元素周期律ppt 第1课时元素周期律 第一ppt



元素周期表 自然百科 百问百科




2 2觀念09價電子數與價數的關係 基礎化學 原子結構與元素週期表 均一教育平台
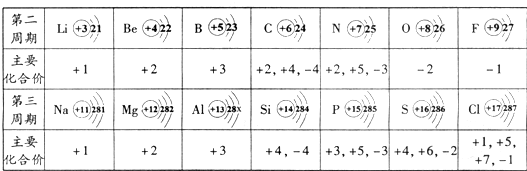



元素周期表的特点及其应用解析 初中化学 新东方在线网络课堂



如果把元素周期表里的元素各买1克 大概需要多少钱 腾讯新闻




元素周期表




2 3觀念01現代週期表簡介 7週期18族 基礎化學 原子結構與元素週期表 均一教育平台



元素周期表和元素周期律



元素周期表上的新元素到底该用哪个汉字命名 中国网友炸开了锅



化学元素周期表规律总结 范文118



高中化学必考点 物质结构 元素周期表详解 抓住考点 把握分数 教育资讯 娱乐新闻网




22届人教版高考化学一轮课时作业15元素周期表和元素周期律 Word版附解析 莲山课件



化学从宏观和微观两个角度认识物质 1 图甲是两种元素在元素周期表 中的信息 图乙是钠原子和氧原子的原子结构示意图 图甲的横线上填的是nana 图乙横线上的数字是66 根据图乙的信息 写出氧化钠的化学式并标出化合价 1na2 2o 1na2 2o 2 下 表所列的是部分元素的有关
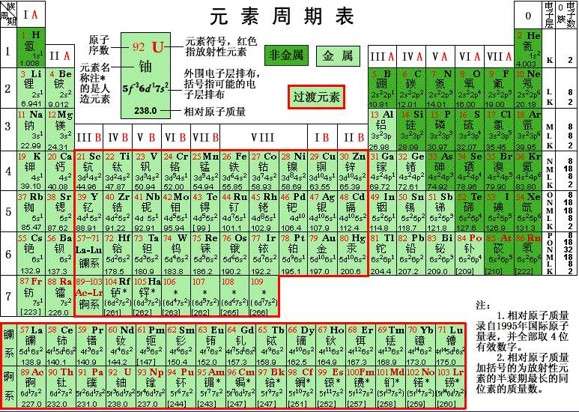



高中化学a12 元素周期表 知乎



化学元素周期表1米x0 78米 分享给大家 西安中考 家长帮




巧用元素周期律和元素周期表规律 参考网




浙江选考 高考化学一轮复习专题五第二单元元素周期表与元素周期律夯基提能作业 人教版高三全册化学试题下载 Word模板 爱问共享资料




17 18学年鲁科版必修2 第1章第3节元素周期表的应用 第2课时 作业 3 302edu教育资源网



广东专供水晶胶化学元素周期表厂家直销 工厂价格 定制加工 报价哪家好 金美工艺制品



元素周期表 科普 大科普网ikepu Com



元素周期表诞生150周年 你还记得几个 知识分子 财新博客 新世纪的常识传播者 财新网




原子價數表 參壹柒 痞客邦



苏教版化学必修二双基限时练 元素周期表及其应用 含答案 莲山课件



周期表化学元素化学电子组态同位素周期png图片素材免费下载 图片编号 Png素材网



元素周期表质量数原子序数化学元素表png图片素材免费下载 图片编号 Png素材网




如何求价电子 12 步骤




元素周期表化学价电子化学元素表图数png图片素材免费下载 图片编号 Png素材网



元素周期律 高中化学知识点




初中化学 元素周期表的 周期 是什么意思 有什么用处 每日头条




Rg元素原子数的伦琴符号周期表中的化学元素周期表库存例证 插画包括有背包 医学




科普贴 为什么常见的化学元素周期表是方形的 分析测试百科网




快速记忆元素周期表 提高5倍速度 延长10倍记忆时长 每日头条




17 18学年鲁科版必修2 第1章第3节元素周期表的应用作业 1 302edu教育资源网
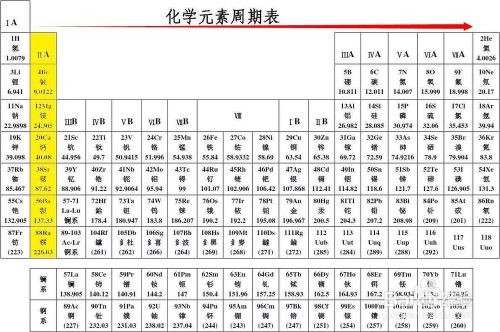



怎么看懂化学元素周期表呢 百度经验



元素周期律和元素周期表 原子结构元素周期律ppt 第1课时元素周期律 第一ppt




化学元素周期表正确使用化学元素周期表的方法




元素周期表中有多少个元素 自然科学21



Search Q Periodic Table E5 85 E7 B4 A0 E5 91 A8 E6 9c 9f E8 A1 A8 Tbm Isch




确定价电子数 建议 July 21



元素周期表 中文百科




初三化学入门知识 元素排列与元素周期表




元素周期表 Ptable



元素周期表技术前沿中国标准物质网




高中化学常见考点值元素周期表 主族 原子 金属性 周期律 网易订阅



高中化学元素周期表专项练习带答案 松鼠文库




Fghgf Fghgf 墙贴 装饰贴包邮元素周期表挂图 化学元素周期表图 校园文化宣传海报挂画 价格图片品牌报价 苏宁易购唯多宝家装建材专营店



化学元素周期表 附元素周期表高清大图 Pdf文件




File 元素周期表 Png 维基教科书 自由的教学读本



元素周期表作用




如果把元素周期表里所有的元素都买1克 大概需要多少钱 比尔盖茨 地壳 化学元素 人工合成 网易订阅




元素周期表同好会 Photos Facebook



化学元素周期表打印版 元素周期表 化学元素列表 23yy




價數歌 Youtube




图片记忆法 教你记住高中化学元素周期表的所有元素 化学还难吗 每日头条




一 原子结构与元素周期表知识回顾元素周期表的结构 Ppt Download




2 2例題01電子的排列方式與價電子數 Youtube




老师推荐 新版118位元素周期表墙贴纸化学元素周期表校园文化初中海报挂图元素表 绿色 118位pp胶 背面带胶 36寸 60x90cm 图片价格品牌评论 京东
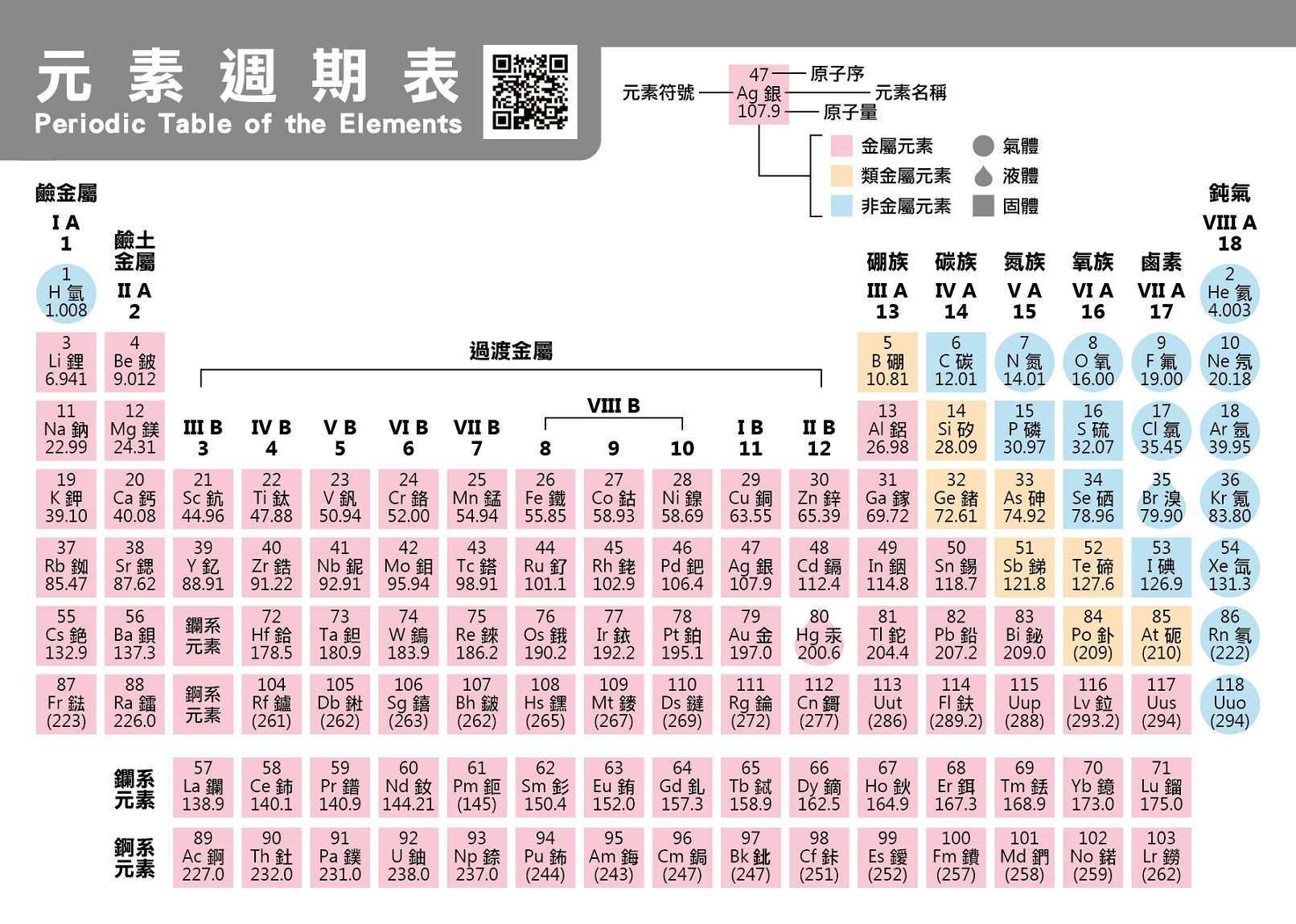



桌遊設計融入化學課程 以元素週期表概念為例 多元教案 授課橘



元素周期律 维基百科 自由的百科全书




科学家推出更新的元素周期表 门捷列夫 大纪元




高一化学必修第一册19版 第四章第一节原子结构与元素周期表 三好网




如何求价电子 12 步骤




化學元素周期表 化學元素周期表是根據原子序數從小至大排序的化學元素列表 百科知識中文網
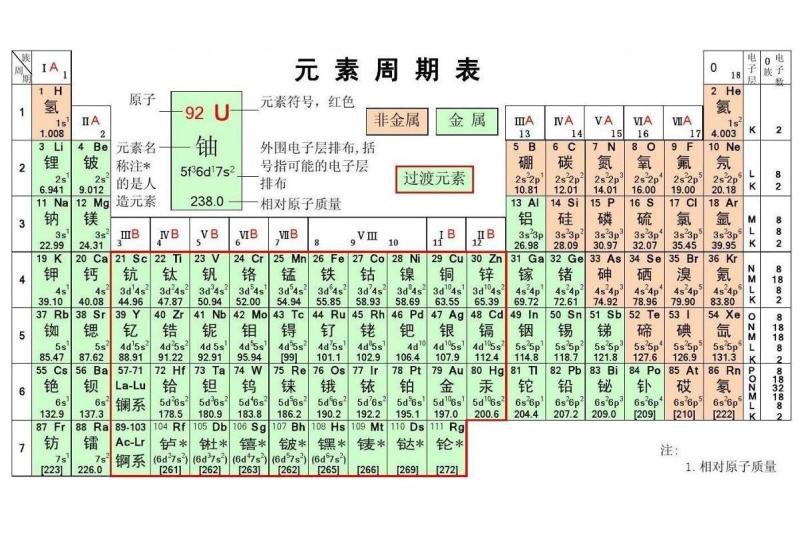



化学元素周期表 俄罗斯化学家门捷列夫总结的化学元素列表 搜狗百科
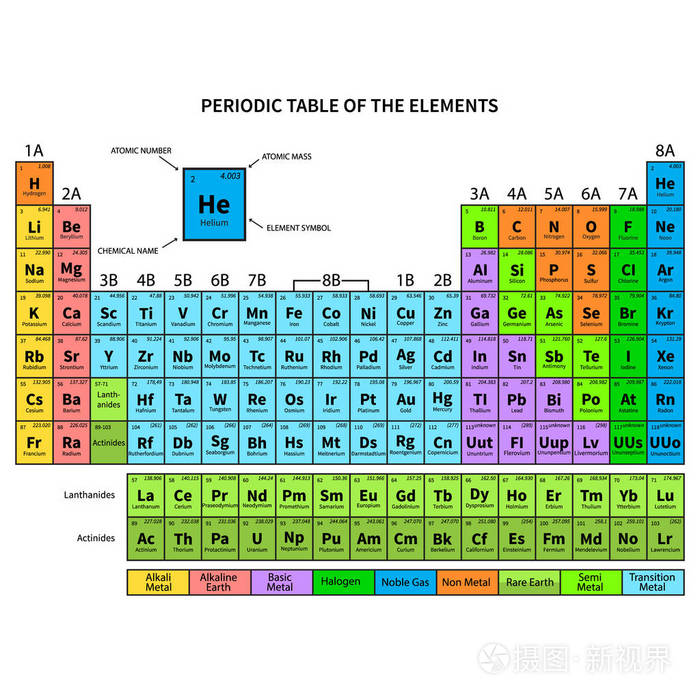



元素周期表 显示原子数 符号 名称和原子重量 矢量插图插画 正版商用图片059pt3 摄图新视界




元素周期表 维基百科 自由的百科全书



高中化学元素周期表6大知识点及其29个误区 电子云




元素周期表高清大图绿色版下载 硒鼓粉盒网



化学元素周期表 附元素周期表高清大图 Pdf文件
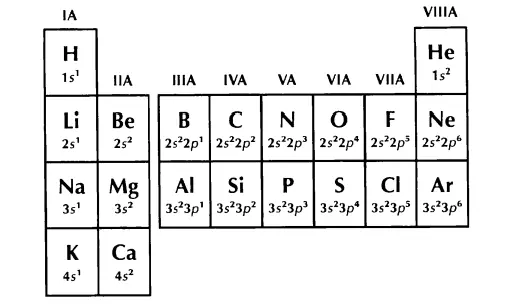



价电子与化合物的分类 哔哩哔哩



解析元素周期表 化学元素周期表有哪些规律 化学元素周期表规律总结 秦学教育




浙江选考 版高考化学一轮复习专题五第二单元元素周期表与元素周期律夯基提能作业下载 Word模板 爱问共享资料




元素周期表 锌库存例证 插画包括有科学 化学 化学制品 要素 健康 瓦片 补充条款



元素周期表是学习和研究化学的重要工具 回答下列问题 1 元素周期表中不同种元素间最本质的区别是 填字母 A 质子数不同b 中子数不同c 相对原子质量不同 2 1869年 立事作业互答平台 专业的学生作业问答网站



Q Tbn And9gcrofuucjwdq7l8xaaqo E51nlh4bex Xcrmjmabneu Usqp Cau




分享 元素週期表periodic Table Of Elements 輕鬆趣味背頌口訣超萌化學元素週期表 化學元素表 背法 之歌 圖文 價數 英文 Pdf 注音 海報 原子量 Word 族 Rd App 偉恩史達克 生活趨勢觀察家



コメント
コメントを投稿